의약품 수출·마일스톤 효과로 해외 실적 ↑녹십자·유한양행·HK이노엔 '신약'이 견인대웅제약 '나보타' 질주 계속···'캔박카스' 회복
국내 주요 제약사들이 의료파업 장기화 등 악조건 속에서도 3분기 호실적을 이어갔다. 의약품 수출, 기술이전에 따른 마일스톤 유입 등 해외 실적이 매출 및 수익성 성장을 견인해서다.
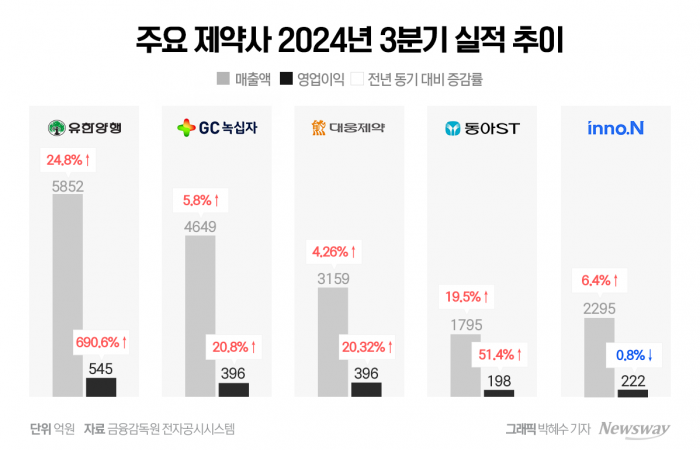
1일 전자공시시스템에 따르면, GC녹십자는 혈액제제 '알리글로'의 미국 시장 진출, 헌터라제 정상 궤도 안착 효과 등으로 3분기 실적이 개선됐다. 연결기준 영업이익은 396억원으로 지난해 동기보다 20.8% 증가했고 순이익은 358억원으로 96.2% 늘었다. 매출은 4649억원으로 같은 기간 5.8% 증가했다.
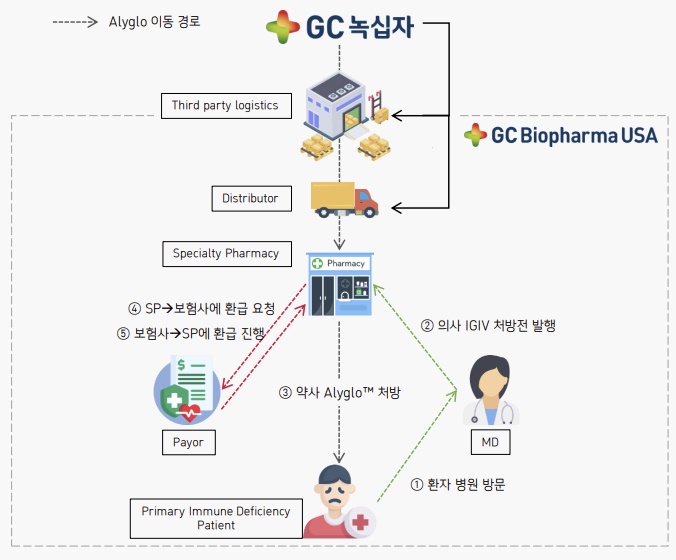
지난해 말 식품의약국(FDA) 허가를 받은 알리글로는 지난 7월부터 미국 공략을 시작했으며, 미국 사보험 시장 80% 이상 확보를 완료해 환자 투여도 순조롭게 진행되고 있다. 특히 대형 스페셜 파머시(SP) 11사와 계약을 체결해 미국 50개 주 전역 판매가 가능해졌으며, 추가 계약 추진으로 물량 확대 및 성장이 기대되는 상황이다.
미국 내 주요 보험사 3곳 중 한 곳인 시그나는 선천적 면역결핍증(PID) 환자 중 동반질환(Comorbidity)이 있는 경우 알리글로를 우선 처방토록 지정했다.
알리글로 미국 매출은 4분기부터 본격적으로 확대돼 내년 약 1500억원 수준으로 성장하고 매년 50% 이상 증가할 것으로 전망된다.
현재 회사는 알리글로의 확장성을 위해 소아 대상의 임상 3상도 진행하고 있다. 임상 완료 목표 시기는 오는 2026년이다.
고마진 품목인 헌터증후군 치료제 '헌터라제'의 수출 정상화도 실적 개선에 영향을 끼쳤다. 헌터라제의 3분기 누계 수출액은 전년 전체 수출의 30%를 달성했다.
회사는 오는 2030년까지 헌터라제 수출국을 29개국으로 확장해 매출을 2배 이상 끌어올리는 것을 목표로 하고 있다. 현재 국내 포함 13개국에 판매 중이다.
유한양행은 렉라자의 글로벌 상용화에 따른 마일스톤 발생으로 실적 개선이 빠르게 이뤄지고 있다. 올 3분기 별도재무제표 기준 회사의 3분기 라이선스 수익은 981억원으로 집계돼 전년 동기(5억원) 대비 1만9494% 폭증했다. 영업이익은 545억원으로 전년 동기 대비 690.6% 성장했고 매출은 5852억원으로 같은 기간 24.8% 늘었다. 당기순이익은 237억원으로 전년 대비 85.1% 증가했다.
렉라자는 지난 8월 미국 존슨앤드존슨(J&J)의 자회사 얀센의 정맥주사(IV) 제형 항암제 '리브리반트'(성분명 아미반타맙)와의 병용요법으로 미국 식품의약국(FDA)의 허가를 받았다. 또 렉라자는 경쟁 약물인 아스트라제네카의 '타그리소'보다 높은 약가를 받기도 했다. 렉라자의 1개월 복용분(30정) 가격은 1만8000달러(약 2400만원)로, 연간으로 환산하면 약 21만6000달러(약 2억9000만원)에 달한다. 타그리소의 미국 내 연간 약가는 20만4000달러(약 2억7000만원)다.
렉라자는 일본·유럽·중국 등 세계 주요 제약 시장에서도 상용화 절차에 돌입한 상태다. 특히 파트너사인 얀센이 리브리반트를 근육에 투여하는 피하주사(SC) 제형으로 개발해 렉라자와 병용하는 요법으로도 추가 허가 신청에 나서고 있어 추가 마일스톤 발생이 기대되는 상황이다. 얀센은 리브리반트 SC제형과 렉라자 병용요법으로 유럽의약품청(EMA)에 허가 신청을 한 한 상황이다. 유럽·중국·일본 등에서 추가 허가를 받을 경우 발생할 마일스톤은 약 1500억원에 달할 것으로 보인다.
대웅제약은 매출 쌍두마차인 보툴리눔 톡신 제제 '나보타'와 국산 34호 신약 '펙수클루'의 글로벌 판매 확대 영향으로 3분기 별도기준 영업이익이 전년 동기 대비 20.32% 증가한 411억원을 기록했다. 매출은 같은 기간 4.26% 늘어난 3159억원이었다.
나보타 매출은 3분기 474억원을 기록했는데, 수출 비중이 약 85%로 나타났다.
그중에서도 전 세계 톡신 시장에서 가장 큰 비중을 차지하고 있는 미국 시장(미국 수출명 주보)에서의 약진이 계속됐다. 나보타는 미국 미용 시장에서 점유율 13%를 차지하며 매출 2위 포지TUS에 안착했다. 나보타의 미국 매출은 올 상반기 기준 프랑스 입센사의 디스포트 실적을 넘어서기도 했다.
나보타의 질주는 계속될 전망이다. 글로벌 보툴리눔 톡신 시장은 오는 2028년까지 연평균 10%씩 증가해 10조원 규모까지 성장할 것으로 예측된다. 나보타는 현재까지 전 세계 68개국에서 품목 허가를 받았고 80여 개국과 파트너십을 체결했다. 최근에는 동남아시아에서 의약품 진출이 가장 까다로운 국가로 알려진 말레이시아에서 제품을 출시했다.
나보타는 중국 허가당국 승인도 앞두고 있어 추가 성장이 기대된다. 중국 보툴리눔 톡신 시장은 2023년 1조4000억원에서 2030년 약 5조원까지 성장할 것으로 추정되는 거대 시장이다. 나보타는 3분기 중국 승인을 위한 공장 실사를 완료했고, 이르면 올해 말 또는 내년 초 승인이 예장된다. 제품 출시는 내년 상반기가 될 것으로 보인다.
위식도역류질환 신약 '펙수클루'도 고성장 품목으로 자리 잡고 있다. 펙수클루는 칼륨경쟁적위산분비억제제(P-CAB) 후발주자임에도 불구하고 높은 시장성과 영업력으로 빠르게 점유율을 높여나가고 있다. 3분기 펙수클루 매출은 226억원으로 전년 동기 대비 57% 증가했으며, 연간 누적 매출은 739억원을 기록해 연매출 1000억원 달성을 기대케 한다. 현재 펙수클루는 종근당이 공동 판매 중이다.
펙수클루의 글로벌 진출도 순항하고 있다. 현재 펙수클루가 출시된 나라는 한국을 포함 필리핀, 멕시코, 에콰도르, 칠레 5개국이다. 품목허가 신청국은 중국과 브라질, 사우디아라비아 등 11개국으로 여기에 인도, 아랍에미리트 등 수출계약을 맺은 14개 나라를 합치면 총 30개국에 달한다.
펙수클루는 나보타와 함께 중국행을 예고하고 있다. 중국 판매 파트너사는 양쯔강의약그룹 자회사 상하이하이니다.
허혜민 키움증권 연구원은 "연말~연초 펙수클루와 나보타의 중국 허가 승인이 예상되고, 나보타의 중국 판매 파트너사 선정 또한 기대된다"며 "대웅제약은 4분기도 무난한 실적을 보일 전망이지만, 중국 신약 승인이 된다면 내년 하반기 실적 추가 상향이 가능하다는 점에서 밸류에이션 매력은 더욱 부각될 것"이라고 평가했다.
동아에스티도 전문의약품(ETC) 사업과 함께 캔박카스 해외사업 호조로 3분기 1795억원의 매출을 기록했다. 이는 전년 동기 대비 19.5% 증가한 수치다. 영업이익은 같은 기간 51.4% 증가한 198억원이었다.
이 중 해외사업 부문 매출액은 캔박카스(캄보디아) 매출의 기저효과 및 판매수량 회복 등의 영향으로 전년 동기보다 47.6% 증가한 460억원을 기록했다. 캄보디아는 캔바카스의 주요 수출국이지만 경기침체로 인해 지난해 매출이 감소한 바 있다. 올해는 221억원의 매출 실적을 내며 전년 대비 63.6% 성장했다.
이밖에도 빈혈치료제 '다베포에틴알파BS'의 수출 매출이 43억원으로 전년 대비 3.0% 증가했고, 인성장호르몬제 '그로트로핀'은 13억원으로 전년 동기 대비 113.5% 증가했다.
다만 결핵치료제 '크로세린'은 15억원의 실적을 내며 전년보다 약 60% 가까이 감소했다.
동아에스티는 R&D 부문을 강화하며 해외 실적 강화에 나설 방침이다.
현재 회사는 글로벌 블록버스터인 스텔라라 바이오시밀러 '이뮬도사'(프로젝트명 DMB-3115, 성분명 우스테키누맙) 사업 개시를 앞두고 있다.
앞서 이뮬도사는 지난달 미국 식품의약국(FDA)의 품목허가를 받았고, 뒤이어 유럽 의약품청(EMA) 산하 약물사용자문위원회(CHMP)로부터 품목허가 승인 권고를 받았다. CHMP 품목허가 승인 권고 의견은 유럽연합 집행위원회(EC)의 최종 승인에 결정적인 역할을 하며, 품목허가 승인 권고 의견 후 EC는 공식 품목허가 여부를 결정한다.
P-CAB 제제 선두주자인 HK이노엔은 케이캡의 수출 증가 등의 영향으로 호실적을 냈다.
HK이노엔은 올 3분기 H&B 사업부문 매출 감소, P-CAB 생산설비 교체에 따른 국내 출하량 일시적 감소 등에 의해 수익성이 소폭 악화됐지만 매출은 전년 동기 대비 6.4% 증가했다. 매출은 2295억원으로 집계됐고, 영업이익은 같은 기간 0.8% 감소한 222억원이었다.
케이캡 수출 매출은 지난 1분기 13억원에서 3분기 21억원으로 증가했고, 연간 누적 약 40억원을 기록했다.
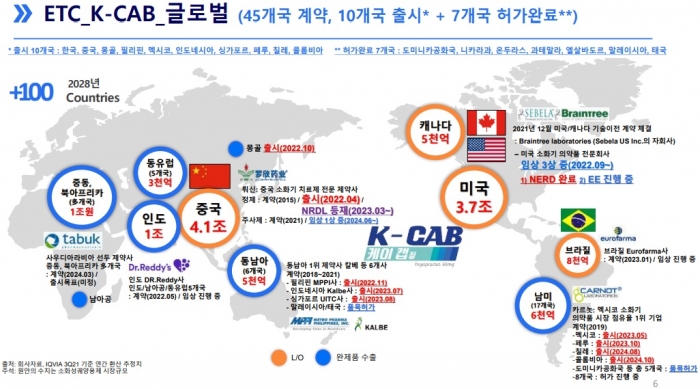
케이캡은 글로벌 시장 진출을 가속화하고 있다. 현재 케이캡은 45개국과 수출 계약을 체결했고, 중국, 필리핀, 인도네시아, 중남미 등 10개국에 출시했다. 최근에는 도미니카공화국, 니카라과, 온두라스, 말레이시아, 태국 등 7개국에서 품목허가를 받아 연내 출시를 앞두고 있다.
회사는 세계 최대 시장인 미국도 공략하고 있다. 파트너사인 세벨라파마슈티컬스를 통해 임상 3상을 진행하고 있으며, 비미란성 식도염으로는 임상을 마친 상태다. 미란성 식도염 적응증 임상은 내년 상반기 종료가 목표다.

뉴스웨이 유수인 기자
suin@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지









댓글