삼진제약이 국내 판매를 맡은 웨어러블 심전도기 '에스패치-EX'(제조사: 웰리시스)가 미국 식품의약국(FDA)의 승인을 받았다.
6일 삼진제약에 따르면, '에스패치-EX'는 지난 2019년 삼성SDS로부터 스핀오프 한 디지털 헬스케어 스타트업 '웰리시스'가 개발/제조한 웨어러블 심전도 솔루션이다.
현재 국내 식품의약품안전처 허가를 포함, 유럽 CE, 호주 TGA, 뉴질랜드 MEDSAFE에 의료기기로 등록돼 있고 전 세계 14개국에 제품 판매 중이다.
이번 미국 FDA 승인으로 '에스패치-EX'는 다시 한번 해외에서의 기술력과 안전성을 입증받게 되는 전기를 마련하게 됐다. 이는 향후 제품 신뢰도 향상 및 국내 시장 점유율 상승에 긍정적인 영향을 끼칠 것으로 기대되고 있다.
'에스패치-EX'는 부정맥 및 심장질환 진단에 필요한 서포트 역할을 한다.
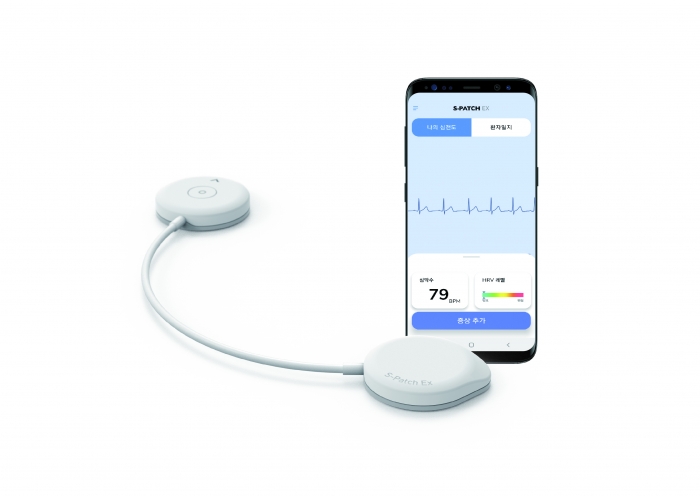
부착 시 높은 착용 편의성과 정확한 진단 결과, 가독성이 우수한 심전도 결과 레포트 제공 등으로 인해 국내 의료진의 부정맥 진단에도 효과적으로 사용되고 있다.
특히 이 제품은 기존 '홀터' 심전도계가 가지고 있던 환자와 의료진의 불편함을 해소시켰다는 점에서 주목받는다. 그간 의료기관에서 사용돼 왔던 '홀터'는 고가의 소프트웨어 구매 및 유지 보수 등으로 효율적인 관리에 어려움이 있었으며 특히, 의료진은 검사받은 환자가 병원에 방문해야만 해당 심전도 데이터 판독이 가능하다는 단점도 있었다.
'에스패치-EX'는 모바일 앱과 기기에서 사용자의 증상 기록이 가능하며, 기록된 증상이 자동으로 소프트웨어에 표시돼 환자 관리가 수월하다는 특장점을 갖추고 있다. 또 검사 종료 후 클라우드 서버로 데이터가 자동 전송되므로 환자가 병원에 기기를 반납하기 전 시간적, 물리적 제한 없는 판독이 가능하다.
삼진제약 헬스케어팀 관계자는 "에스패치-EX의 미 FDA 승인은 웨어러블 심전도 검사 시장 중 최대 규모로 평가받는 미국에서 제품의 안전성과 유효성을 인정받았다는데 큰 의미가 있다"고 전했다.

뉴스웨이 유수인 기자
suin@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지









댓글