약 10조원 규모 美 의료AI 시장 진출 러쉬 뷰노·루닛·코어라인소프트·제이엘케이 등 양질 데이터 보유, 높은 기술력에 '글로벌 선도' 가능성
국내 의료 인공지능(AI) 기업들이 세계 최대 의료 시장인 미국 진출을 가속화하고 있다. 업계는 한국 의료AI 기업들의 기술력이 전 세계적으로 인정받고 있는 만큼 빠른 시장 안착을 기대하고 있다.
16일 글로벌 시장조사업체 프레시던스 리서치에 따르면 지난 2022년 기준 전 세계 의료AI 시장 규모는 151억 달러(21조841억원)로, 이 중 북미 시장 규모가 68억 달러(9조4948억원)를 차지하는 것으로 알려진다.
글로벌 의료AI 시장은 연평균 37%씩 성장할 것으로 예상되고 있어 북미 지역에서의 성장세도 가파를 것으로 전망된다. 오는 2030년 예상 시장 규모는 1879억5000만달러(약 260조원)다.
이미 국내외에서 기술력을 입증한 국내 의료AI 기업들은 세계 최대 시장을 선점을 위해 진출을 서두르고 있다.
'뷰노메드' 美 진출 추진···심전도 측정기 '하티브'에도 AI 솔루션 탑재
국내 1호 AI 의료기기를 선보인 뷰노는 자체 개발 솔루션인 '뷰노메드' 시리즈 4종과 심전도 측정 의료기기를 미국 시장에 선보이기 위해 속도를 내는 중이다.
상용화가 가장 빠른 솔루션은 AI기반 뇌 정량화 의료기기 '뷰노메드 딥브레인'이다. 딥브레인은 지난해 10월 미국식품의약국(FDA) 인증을 획득했으며, 올해 중순 공식 런칭을 목표하고 있다.
현재 회사는 빠른 시장안착을 위해 현지 시장 조사, 사전 마케팅 전략 기획 등을 진행 중이다. 특히 지난해 알츠하이머 치료제의 등장으로 치매 조기 진단 시장의 가파른 성장이 기대되고 있어 AI를 활용한 치매 조기 진단에 대한 수요가 커질 것으로 회사측은 기대하고 있다.
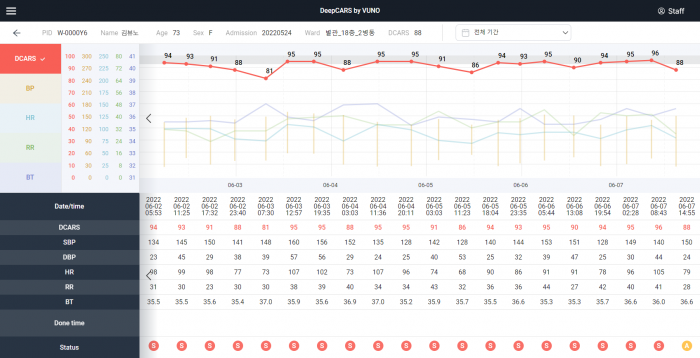
다음으로는 심정지 예측 솔루션 '뷰노메드 딥카스'가 있다. 딥카스는 올 하반기 FDA 인증, 2025년 초 런칭을 목표로 하고 있으며, 최근 미국 상표권 등록(DeepCARS®)도 완료했다.
딥카스는 국내 의료시장에서 큰 성과를 거두고 있으며, 시장성과 혁신성을 인정받아 국내 의료 AI 업계 최초로 FDA 혁신의료기기 지정을 받기도 했다. 회사는 이같은 사례 바탕으로 미국 시장에서 영업 및 마케팅을 전개한다는 방침이다.
회사측은 "현재 일반병동 입원환자의 심정지를 예측하는 AI기반 의료기기는 딥카스 외에 확인되는 제품이 없다"며 "이에 딥카스는 미국 병원 내 입원 환자의 안전관리에 기여하는 '필수의료'의 성격을 갖는 제품으로서 시장에서 수요를 가질 수 있을 것으로 예상된다"고 전했다.
이밖의 흉부 CT 판독 보조 솔루션 '뷰노메드 흉부 CT AI'도 내년 하반기 FDA 인증을 목표로 하고 있다. 이를 위해 회사는 미국 하버드 의대 부속병원인 MGH와 인허가 획득을 위한 임상연구를 수행하고 있다.
이 제품은 현재 폐 CT 시장 수요가 큰 일본 시장에서 해외 파트너사와 협력해 사업성과를 늘리고 있으며, 사업성과 입증 후 미국 시장에 진출할 계획이다.
AI 기반 흉부 엑스레이 판독 보조 솔루션 '뷰노메드 체스트 엑스레이'도 미국 시장 진출을 위한 인허가 획득을 추진하고 있으며, 심전도 측정 의료기기 '하티브' 또한 내년 중순 FDA 인허가를 위해 미국 상표권 등록(Hativ®)를 완료했다. 특히 회사는 하티브에도 AI 기반 심혈관 질환 탐지 소프트웨어를 탑재해 경쟁력을 갖출 예정이다.

현지 유통망 확보 나선 루닛···'볼파라' 인수로 세일즈 강화
루닛은 미국 시장 장악을 위해 현지 영업망이 탄탄한 뉴질랜드 기업 볼파라헬스테크놀로지(이하 볼파라) 인수를 추진하고 있으며, 현재 마무리 단계에 접어들었다.
볼파라는 유방암 검진에 특화된 AI 플랫폼 기업으로, 미국 시애틀에 사무소를 두고 현지 시장을 집중 공략하고 있다. 이에 미국 전체 유방촬영술 검진기관의 3분의 1에 해당하는 2000곳 이상 의료기관에서 볼파라 제품을 사용하고 있다. 회사 전체 매출의 96.5%는 미국에서 발생하고 있다.
루닛이 볼파라를 인수한 건 자사 AI 솔루션의 품목허가가 늦어지면서 현지 시장 진출이 지연됐기 때문이다. 루닛의 3차원(3D) 유방단층촬영술 AI 영상분석 솔루션 '루닛 인사이트 DBT'는 지난해 11월 FDA로부터 시판 전 허가(510(k) Clearance)를 받았다.
루닛은 볼파라 인수로 전 세계 유방암 검진 시장의 65%를 차지하는 미국 시장 진출에 속도를 내겠단 방침이다.
서범석 대표는 작년 12월 개최한 기자간담회에서 "미국은 우리가 가장 부족한 시장이지만 볼파라가 이미 현지에서 브랜딩이 잘돼있고 입지도 탄탄해 같이 비즈니스를 한다면 진출 시기를 앞당길 수 있을 것 같았다"며 "이 회사 제품을 쓰고 있는 미국 내 의료기관은 42%에 달한다. 우리에겐 유통채널이 확보된 셈"이라고 강조했다.

코어라인소프트·JLK도 진출 속도···업계 "전세계 韓기업 주목"
코어라인소프트는 지난 2018년 AI 기반 통합 제품군인 'AVIEW'로 FDA 최초 인증을 획득한 이후 지금까지 총 9개 제품에 대해 미국 허가를 받았다.
특히 지난해 FDA 510(k) 인허가를 획득한 'AI 폐결절 검출보조 소프트웨(CAD)'는 국산 제품으로는 최초로, 전세계적으로는 다섯 번째로 미국 허가를 획득했다.
이 솔루션은 FDA에서 허가한 기존 제품들과 다르게 폐암검진 목적으로 시행한 저선량 흉부 CT 외의 다른 목적으로 시행한 일반 흉부 CT에서도 효과를 인정받아 주목을 받고 있다.
최근에는 AI 기반 관상동맥 석회화 자동 진단솔루션 'AVIEW CAC'도 FDA로부터 510(K) 인증을 받았다. 현재 미국에서는 관상동맥석회화의 위험도를 분류해주는 제품에 대해 임시수가코드에 해당하는 'CPT 코드'를 부여하는 등 가치를 인정해주고 있어 해당 솔루션의 경우에도 실제 임상에서 적극 활용될 것으로 기대를 모으고 있다.
회사는 미국법인을 통해 현지 영업도 확대하고 있다.
앞서 회사는 지난 2021년 하반기 북미 법인 설립 후 UCLA 하버, 스탠포드 의과대학 3D 실험실, UMMH(UMass Memorial Health)등과 제품 판매 및 연구협력을 진행하고 있다.
제이엘케이(JLK)는 올해를 미국 진출 원년으로 삼고 'JBS-04K', 'JBS-LVO' 등 일부 솔루션에 대한 FDA 인허가 절차를 계획 중이다. 미국은 이미 뇌졸중 관련 AI 시장이 구축돼 있고, 경쟁사보다 민감도, 특이도가 높은 제품 솔루션을 보유하고 있어 현지 시장 진출 후 빠른 점유율 확대가 가능할 것으로 회사 측은 보고 있다.
현재 원활한 시장 진출을 위해 유나이티드헬스케어, 체인지헬스케어 등 현지 대형 의료보험사, 호간 등 리테일 마케팅 전문 업체 등과 협의를 진행 중인 것으로 알려진다.
한편, 의료AI 업계는 현재 전 세계적으로 한국 기업에 대한 주목도가 올라가고 있어 미국 시장에서도 입지를 빠르게 넓혀나갈 수 있을 것으로 기대하고 있다.
한 업계 관계자는 "한국 의료AI에 대한 세계적인 관심과 신뢰는 매우 높은 상황"이라며 "우선 의사들이 경쟁력을 갖추고 있고, 환자가 많은 대형병원들이 수도권에 밀집돼 있어 양질의 데이터를 확보할 수 있다는 점에서 AI 의료기기를 개발하는 데 유리하기 때문"이라고 설명했다.
이 관계자는 "최근 시장성을 입증하며 임상적 가치를 쌓고 있는 제품이 속속 등장하고 있다. 글로벌 선도 기업은 한국에서도 충분히 등장할 수 있을 것으로 보고 있다"고 말했다.

뉴스웨이 유수인 기자
suin@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지









댓글