중대한 이상사례 검토‧처리 지침서, 장기추적조사 지정 해제 절차 마련
식품의약품안전처는 첨단바이오의약품 장기추적조사를 체계적으로 운영하기 위한 '중대한 이상사례 검토‧처리 지침서'와 '장기추적조사 지정 해제 절차'를 마련했다고 31일 밝혔다.
첨단바이오의약품 장기추적조사는 줄기세포 또는 유전물질을 포함한 첨단바이오의약품을 투여받은 환자의 안전을 위해 투여 후 장기간에 걸쳐 이상사례 발생 여부를 추적‧조사하는 것을 말한다.
지난 2020년 8월 첨단재생바이오법 시행에 따라 장기추적조사 실시자는 중대한 이상사례가 발생할 경우 이에 대한 조사‧분석 계획을 수립하고 그 결과를 식약처에 제출해야 한다. 줄기세포치료제는 5년, 유전자치료제는 15년, 이종이식제제는 30년간 추적‧조사한다.
식약처는 국내 제약사, 개발사가 장기추적조사 계획을 수립‧실시하는 데 도움을 주기 위해 해당 업무의 처리 절차를 안내한 '중대한 이상사례 검토‧처리 지침서'를 마련했다.
지침서 주요 내용은 ▲관련 규정‧가이드라인 ▲적용범위 ▲용어 정의 ▲검토 자료‧절차 흐름도 등 검토지침 ▲접수‧검토‧보완‧결과회신 등 검토 절차이다.
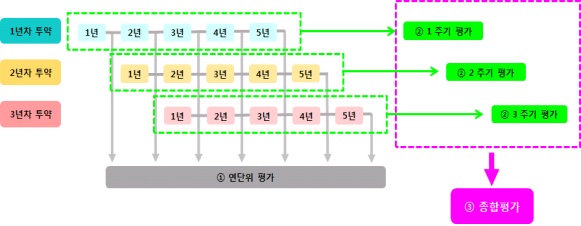
또 추적‧평가 3주기가 종료된 첨단바이오의약품의 장기추적조사 결과를 종합적으로 평가하여 장기추적조사 지속 여부를 결정하도록 하는 '장기추적조사 지정 해제 절차'도 마련했다.
주요 내용은 ▲지정해제 검토대상 ▲평가자료 ▲종합평가‧지정해제 절차 등이며, 향후 안정적인 운영을 위해 '첨단바이오의약품 장기추적조사 관리기준'(식약처고시)에도 해당 절차를 반영할 계획이다.
식약처는 "앞으로도 규제과학을 바탕으로 장기추적조사 제도를 합리적으로 운영하며 첨단바이오의약품 안전을 더욱 철저히 관리하겠다"고 전했다.

뉴스웨이 유수인 기자
suin@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지









댓글