
제약·바이오
블랙록이 점찍은 코스닥 바이오···HLB '간암 신약' 기대감 재부각
블랙록 펀드 어드바이저스가 HLB 지분 5.01%를 확보하며 2대 주주에 올랐다. HLB의 미국 FDA 신약 허가 심사 일정과 맞물려 시장 관심이 높아졌다. 블랙록은 패시브 투자자로서 경영 참여보다는 스튜어드십 원칙을 적용할 전망이다. HLB는 ESG 등급과 재무 구조 개선 등 과제가 남아 있다.
[총 115건 검색]
상세검색

제약·바이오
블랙록이 점찍은 코스닥 바이오···HLB '간암 신약' 기대감 재부각
블랙록 펀드 어드바이저스가 HLB 지분 5.01%를 확보하며 2대 주주에 올랐다. HLB의 미국 FDA 신약 허가 심사 일정과 맞물려 시장 관심이 높아졌다. 블랙록은 패시브 투자자로서 경영 참여보다는 스튜어드십 원칙을 적용할 전망이다. HLB는 ESG 등급과 재무 구조 개선 등 과제가 남아 있다.

제약·바이오
HLB, 리보세라닙 재도전 속 '차세대 성장 축' 띄운다
HLB는 간암 1차 치료제 리보세라닙·캄렐리주맙 병용요법의 신약허가를 미국 FDA에 세 번째로 재신청했다. 파이프라인 리스크 분산을 위해 표적항암제 리라푸그라티닙도 추가해 담관암 등 희귀암 시장 확장 전략을 추진하며, 주요 임상 성과와 함께 글로벌 시장 진출을 가속하고 있다.

제약·바이오
HLB, 간암 신약 FDA 허가 재신청
HLB와 자회사 엘레바, 파트너 항서제약이 간암 신약 리보세라닙·캄렐리주맙 병용요법의 미국 FDA 허가 재신청을 완료했다. 해당 치료제는 글로벌 임상 3상에서 간세포암 환자 대상 생존기간 23.8개월을 확인하며 우수한 효능과 안전성을 입증했다. 이번 재신청은 보완사항 반영과 자료 재점검을 거쳐 진행됐다.

제약·바이오
HLB그룹, 김태한 전 삼성바이오 대표 바이오 총괄 회장으로 영입
HBL그룹이 김태한 전 삼성바이오 대표를 영입하며 글로벌시장 확대 전략을 강화했다. HLB그룹은 김태한 전 삼성바이오로직스 대표이사를 바이오 부문 총괄 회장으로 영입한다고 31일 밝혔다. 이번 인사는 바이오 부문 계열사의 연구개발 성과를 그룹의 구조적 성장 체계로 연결해 글로벌 경쟁력을 강화하려는 목적이다. HLB의 전략적 포커스는 R&D와 글로벌 상업화 역량 통합에 맞춰져 있다. 통합 HLB는 항암제 중심 경쟁력에 펩타이드 기

제약·바이오
'통합 HLB' 출범 앞두고 경영·지배구조 재편···진양곤 회장 영향력 견고
HLB그룹이 통합 HLB 출범을 앞두고 김홍철을 신임 대표로 내정하며 경영체제와 지배구조를 재편한다. 진양곤 회장은 대표직에서 물러나지만 지분 기반 영향력은 유지한다. 이번 변화는 글로벌 항암제 시장 공략과 FDA 신약 허가 재도전에 초점을 맞추고 있다.

제약·바이오
위기의 HLB, 사이언스 흡수합병 '승부수'
HLB가 HLB사이언스를 흡수합병해 신약 개발의 어려움과 사업 포트폴리오 단일화 위기를 극복하려는 전략을 내놨다. FDA 승인 두 차례 실패와 HLB생명과학 합병 무산 등 악재 속에서, 펩타이드 기반 신약 등 파이프라인을 확장해 주주가치 및 기업경쟁력 강화를 노리고 있다.
제약·바이오
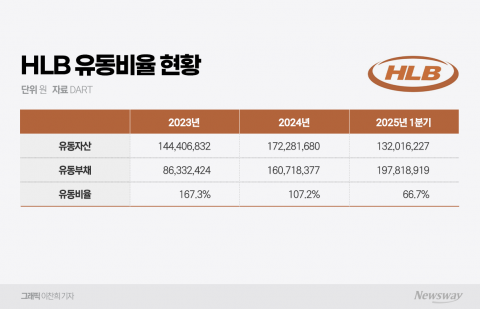
HLB, 간암 표적항암제 승인 재신청···투자자 '촉각'
HLB가 간암 신약의 미국 FDA 허가를 위한 세 번째 도전을 진행 중이다. FDA와의 최근 미팅에서 추가 자료 제출이 요청됐고, 승인 절차가 지연되고 있다. 신약 허가 실패 시 전환사채(CB) 상환 부담 등 재무 리스크가 커질 전망이며, HLB의 유동성 악화와 자금 조달 전략이 시장의 주요 관심사로 부상하고 있다.

제약·바이오
신약 난관 봉착 HLB, 하반기 신약 허가·CAR-T가 반전 열쇠
HLB그룹이 신약 '리보세라닙+캄렐리주맙'의 FDA 승인과 NK치료제 임상 실패로 악재를 겪고 있다. 시장에서는 하반기 담관암 치료제 '리라푸그라티닙'의 조건부 허가와 CAR-T 치료제 임상 1상 데이터 공개에 기대를 걸고 있으며, FDA 승인을 위한 전략 수정과 파이프라인 재정비가 주목받는다.

제약·바이오
존재감 키우는 HLB그룹 계열사들···시너지 '주목'
HLB그룹의 계열사인 HLB제넥스, HLB펩, HLB뉴로토브는 기술 협업을 통해 난치성 질환, 실버 사업 등에서 시너지를 모색하고 있다. 효소 및 펩타이드 기반 기술을 바탕으로 B2B에서 B2C로 시장을 확장하고, 혁신적인 신약 개발에 박차를 가하고 있다. 이들은 IR을 통해 사업 전략 및 기대효과를 발표, 시장의 주목을 받고 있다.

종목
HLB, HLB생명과학 흡수합병
코스닥 상장사 HLB가 자회사 HLB생명과학을 흡수합병한다고 1일 공시했다. HLB의 최대주주는 지분 7.23%를 보유하고 있는 진양곤 대표이사다. 소멸회사인 HLB생명과학 최대주주는 지분 16.98%를 보유하고 있는 존속회사인 HLB이다. 본 합병 완료 이후, 합병회사인 에이치엘비(주)의 최대주주 지분은 7.23%에서 6.63%로 변동된다. 합병가액은 HLB가 5만8349원, HLB생명과학이 6812원으로 합병비율은 1대 0.1167458로 책정됐다. 합병 목적에 대해