
종목
브릿지바이오 임상 실패에 메자닌 투자자들 날벼락
브릿지바이오테라퓨틱스는 특발성 폐섬유증(IPF) 치료제 BBT-877의 임상 2상에 실패하며 주가가 급락하고 있다. 메자닌 투자자들의 손실이 우려되는 가운데, 기술이전 계획을 재추진 중이다. CPS 발행 후 주가는 지속 하락하며 차익 실현에 난항이 예상된다.
[총 21건 검색]
상세검색

종목
브릿지바이오 임상 실패에 메자닌 투자자들 날벼락
브릿지바이오테라퓨틱스는 특발성 폐섬유증(IPF) 치료제 BBT-877의 임상 2상에 실패하며 주가가 급락하고 있다. 메자닌 투자자들의 손실이 우려되는 가운데, 기술이전 계획을 재추진 중이다. CPS 발행 후 주가는 지속 하락하며 차익 실현에 난항이 예상된다.

종목
[특징주]'임상 2상 실패' 브릿지바이오테라퓨틱스, 이틀 연속 '下'
브릿지바이오테라퓨틱스가 개발 중인 특발성 폐섬유증 치료제 후보물질 BBT-877이 글로벌 임상 2상에서 유효성을 입증하지 못해 주가가 이틀 연속 하한가로 떨어졌다. 지난 14일 임상시험 결과 발표 후 투자심리가 급속히 위축되며 주가가 29.94% 급락했다.

제약·바이오
폐섬유증 치료제 지각변동···'브릿지바이오'에 쏠리는 눈
특발성 폐섬유증(IPF) 시장에 지각변동이 일면서 브릿지바이오테라퓨틱스에 관심이 쏠리고 있다. 현재 임상2상 단계에 있는 'BBT-877'의 임상이 순항하고 있고, 개발 경쟁 환경도 우호적으로 조성되고 있어 기술이전 성과 기대감이 높아지는 모습이다. 특히 오는 4월 톱라인 발표를 앞두고 있어 그 이후부터 기술이전 타진을 본격화할 것으로 보인다 13일 글로벌 의약품 시장 분석기관 퍼스트워드파마(Firstword Pharma)에 따르면, 로슈는 최근 IPF

제약·바이오
브릿지바이오 "특발성폐섬유증 신약 美 임상2상 지속 권고···사업화 매진"
브릿지바이오테라퓨틱스는 지난 8일(미국 시간) 개최된 제4차 독립적 자료 모니터링 위원회(이하 'IDMC')로부터 특발성 폐섬유증(IPF) 치료제 후보물질 BBT-877의 제2상 임상시험을 지속하도록 권고 받았다고 10일 밝혔다. 지난 4월의 제3차 IDMC에 이어 네 번째로 개최된 이번 회의에서는 9월 2일을 기준으로 집계된 시험대상자 전체의 유효성 및 안전성 데이터를 검토했다. 그 결과 전문가들은 이전 회의 결과와 동일하게 약물의 안전성 및 효

제약·바이오
브릿지바이오 'BBT-877' 개발 힘 붙는다···"환자모집 완료"
브릿지바이오테라퓨틱스는 특발성 폐섬유증 치료제 후보물질 'BBT-877'의 제2상 임상시험에서 목표로 한 120명의 환자 등록을 완료했다고 30일 밝혔다. 현재 선별 검사 단계에 있는 환자들의 추가 등록 가능성을 고려해 최종 125명 이상의 환자 데이터가 확보될 전망이다. BBT-877의 이번 임상시험은 한국과 미국, 호주, 폴란드, 이스라엘의 50여 개 기관에서 진행되고 있다. 총 120명의 환자에게 24주 동안 시험약 또는 위약을 투여하여 약물의 유효성, 안

제약·바이오
브릿지바이오, 215억 원대 자금 확보···'BBT-877' 개발 가속화
브릿지바이오테라퓨틱스는 지난 17일부터 이틀간 실시한 주주배정 유상증자에서 구주주 청약률 104.5%를 달성해 실권주 없이 공모 절차를 마무리하고 215억 원대의 자금조달을 최종 확정지었다고 19일 공시했다. 회사는 지난 4월 주주배정 유상증자 결의 이후 이달 12일 최종 발행가액 산정을 통해 200억 원대의 자본 조달을 확정지었다. 이번 증자를 통해 신규 조달된 자금은 대부분 BBT-877(특발성 폐섬유증 치료제 후보물질) 및 BBT-207(비소세포폐암 치
제약·바이오
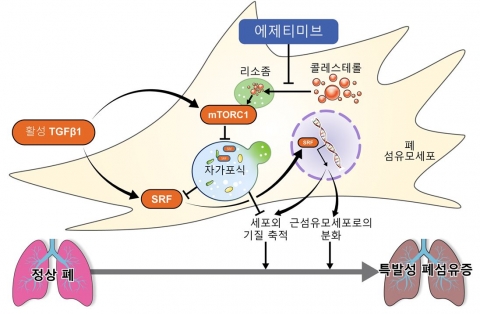
특발성 폐섬유증, '항콜레스테롤제' 복용시 사망 위험 최대 62% ↓
항콜레스테롤 약제 '에제티미브'가 폐섬유증 진행을 억제할 수 있다는 연구결과가 나왔다. 세브란스병원 호흡기내과 김송이 교수·이찬호 강사, 용인세브란스병원 호흡기·알레르기내과 곽세현 교수, 연세대 의과대학 의생명과학부 배수한 교수 연구팀은 특발성 폐섬유증 환자가 에제티미브를 복용하면 사망 위험이 최대 62% 떨어진다고 17일에 밝혔다. 이번 연구 결과는 국제학술지 '유럽 호흡기 저널'(European Respiratory Journal, IF 24.9)에 게재됐다. 폐
![[인터뷰]이정규 대표 "'BBT-877' 풀베팅, 빅파마 관심 뜨거웠다···기술이전 속도낼 것"](https://nimage.newsway.co.kr/photo/2024/06/11/20240611000067_0480.jpg)
제약·바이오
[바이오USA][인터뷰]이정규 대표 "'BBT-877' 풀베팅, 빅파마 관심 뜨거웠다···기술이전 속도낼 것"
"빅파마 관심요? 뜨겁다고 할 수 있죠. 특발성폐섬유증(IPF)에 관심 없던 제약사들의 관심이 많아졌습니다. 좋은 치료제가 없고 생각보다 환자도 많아서 그런 것 같아요. 'BBT-877' 임상 환자 모집이 빠르게 이뤄진다는 건 의사들이 긍정적으로 보고 있다는 얘기입니다. 임상 속도를 최대한 높여서 이를 기반으로 기술이전 협상에 탄력을 얻으려고 합니다." 지난 4일(현시지간) 미국 샌디에이고 '2024 바이오 인터내셔널 컨퍼런스'(이하 바이오USA) 현

제약·바이오
일동제약그룹, 美서 '특발성 폐섬유증 신약' 연구 성과 공개
일동제약그룹의 신약 연구개발 회사 아이리드비엠에스(iLeadBMS)는 미국 흉부학회(ATS 2024)에서 특발성 폐섬유증 치료제 'IL1512'에 관한 연구 성과를 포스터 발표를 통해 공개했다고 21일 밝혔다. 특발성폐섬유증은 폐실질의 섬유화가 점점 진행되는 간질성 폐렴(ILD)의 일종으로, 진단 후 5년 생존율이 40% 미만인 난치성 희귀 질환이다. 글로벌 시장조사기관 리서치앤마켓에 따르면 2030년 시장 규모는 약 61억 달러(한화 약 8조원)에 이를 것으로

제약·바이오
브릿지바이오, 제2차 IDMC서 'BBT-877' 지속 개발 권고
브릿지바이오테라퓨틱스는 독립적인 자료 모니터링 위원회(IDMC)로부터 특발성 폐섬유증(IPF) 치료제 후보물질 'BBT-877'의 제2상 임상시험을 지속하도록 권고 받았다고 30일 밝혔다. 이번 IDMC는 임상시험 대상자 모집이 가속화됨에 따라 지난 해 10월에 이어 약 3개월만에 두 번째로 개최됐다. 북미, 유럽, 아시아 지역 등에서 진행 중인 'BBT-877' 2상 임상시험의 중간 데이터를 토대로 약물의 안전성 및 효능을 검토하고 임상시험의 지속