
제약·바이오
탈모시장 임상 러시···중외·올릭스에 세포치료제까지 가세
국내 제약·바이오업계가 탈모치료제 개발에 박차를 가하고 있다. JW중외제약을 비롯한 기업들이 모낭 줄기세포, RNA 간섭, 세포치료 등 혁신 기전으로 임상시험을 진행 중이며, 건강보험 확대 논의도 시장 성장에 큰 영향을 미치고 있다. 기존 탈모치료제의 한계를 극복하며 신약과 기능성 화장품까지 다양한 분야에서 경쟁이 심화되는 양상이다.
[총 41건 검색]
상세검색

제약·바이오
탈모시장 임상 러시···중외·올릭스에 세포치료제까지 가세
국내 제약·바이오업계가 탈모치료제 개발에 박차를 가하고 있다. JW중외제약을 비롯한 기업들이 모낭 줄기세포, RNA 간섭, 세포치료 등 혁신 기전으로 임상시험을 진행 중이며, 건강보험 확대 논의도 시장 성장에 큰 영향을 미치고 있다. 기존 탈모치료제의 한계를 극복하며 신약과 기능성 화장품까지 다양한 분야에서 경쟁이 심화되는 양상이다.

제약·바이오
'실적 개선' 지씨셀, '이뮨셀엘씨주' 캐시카우로 키운다
지씨셀이 검체 서비스 위주 사업에서 탈피해 세포치료제 '이뮨셀엘씨주' 중심으로 구조를 재편하고 있다. 2023년 영업손실을 전년보다 31% 줄였으며, 인도네시아 등 해외 시장으로 진출을 확대한다. 다양한 암종 임상 연구와 기술수출로 사업 다각화를 모색한다.

제약·바이오
박셀바이오-바이오디자인랩 맞손···'CAR-NK 치료제' 개발 속도 높인다
박셀바이오는 바이러스 벡터 설계 기업 바이오디자인랩과 자가면역질환 치료를 위한 CAR-NK 치료제 공동 개발 업무계약을 체결했다고 23일 밝혔다. 앞서 박셀바이오는 바이오디자인랩, 삼성서울병원 등과 업무협약(MOU)을 맺어 새로운 CAR-NK 치료제 연구개발을 수행해 왔다. 이 같은 업무협약이 가시적 연구성과로 나타남에 따라 개발 속도를 높이기 위해 이번 업무계약을 체결한 것이다. 이번 계약에 따라 박셀바이오는 3세대 NK세포를
제약·바이오
저출산에도 '제대혈' 사업 흥행···'캐시카우' 된 비결은
"제대혈 채취부터 운송, 검사, 보관에 이르는 모든 프로세스를 자체적으로 진행하는 것이 우리의 경쟁력입니다. 경쟁 업체보다 저렴하고 안전하다는 측면 때문에 국내 3위까지 올라섰습니다." 허준영 GC셀(지씨셀) 제대혈사업팀 팀장은 지난 12일 경기도 용인에 위치한 셀센터에서 만나 이같이 말하며 자사의 경쟁력을 강조했다. 제대혈은 분만 시 산모와 태아를 연결하는 탯줄에서 단 한 번 밖에 채혈할 수 없는 혈액을 말한다. 제대혈에는 조혈모세포와

제약·바이오
세브란스, 난치성 말초동맥질환자 대상 세포치료제 임상연구 착수
난치성 심혈관질환인 말초동맥질환 환자에 대한 줄기세포치료 연구가 최근 첨단재생의료 연구 적합 승인을 받았다. 22일 연세대 세브란스병원에 따르면, 병원이 제출한 '말초동맥질환 환자를 대상으로 자가 유도만능줄기세포 유래 혈관내피세포를 투여해 치료하기 위한 고위험 임상연구'가 최근 보건복지부 첨단재생의료 및 첨단바이오의약품 심의위원회와 식품의약품안전처로부터 승인을 받았다. 이번 연구에는 세브란스병원 심장내과 고영국 교수 연

제약·바이오
메디포스트, 세포치료제 등 국내 CDMO 수주 2건 성공
메디포스트는 올 들어 두 건의 위탁개발생산(CDMO) 수주계약을 체결하고 본격적인 공장 가동에 나섰다고 19일 밝혔다. 회사는 이번 계약을 토대로 추가적인 계약에 박차를 가할 계획이다. 메디포스트는 지난 2022년 말 GMP생산시설 내 CDMO 전용 클린룸 및 생산시설 등을 마련하고 CDMO 사업에 진출한다고 밝힌 바 있다. 이번 두 건의 수주계약은 면역세포치료제 임상시험용의약품 위탁생산과 인체 제대혈 세포배양액 공급계약으로 총 금액
제약·바이오
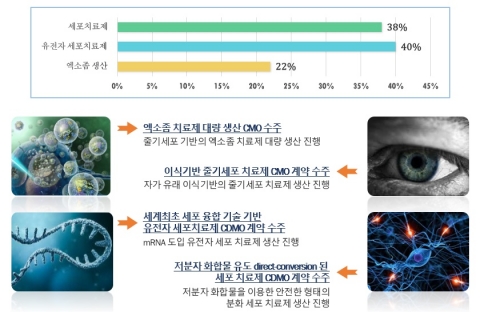
강스템바이오, 세포치료제 CDMO사업 순항···"올해 20억 초과 예상"
강스템바이오텍의 세포치료제 위탁개발생산(CDMO) 사업이 순항하면서 새로운 캐시카우로 부상할 수 있을지 주목된다. 18일 관련 업계에 따르면, 강스템바이오텍은 지난 2020년 12월 첨단바이오의약품 제조업 허가를 받으며 세포치료제 기반 CDMO 사업을 시작했다. 현재까지 총 4개의 프로젝트를 수주해 2022년 기준 총 계약규모는 50억원에 달한다. CDMO사업을 통한 매출액은 2021년 2억2400만원에서 이듬해 8억3900만원으로 4배 가까이 뛰었다. 전체

제약·바이오
GC셀 美 관계사, '루푸스 신염 병용요법' FDA 패스트트랙 지정
GC셀(이하 지씨셀)은 자사의 미국 관계사 아티바바이오테라퓨틱스(이하 아티바)가 개발 중인 루푸스 신염(LN) 치료제 'AlloNK(개발 코드명: AB-101)'이 '리툭시맙(Rituximab)' 또는 '오비누투주맙(Obinutuzumab)'과 병용요법으로 미국 식품의약국(FDA)으로부터 패스트트랙(Fast track) 지정을 받았다고 23일 밝혔다. 이는 지난 8월 아티바가 FDA로부터 최초로 승인을 받은 자가면역질환에서 동종 CAR-T 또는 NK(자연살해)세포치료제의 임상시험
제약·바이오
데이터 쌓고 개발 불확실성 줄이고···바이오업계 '첨생법 개정안' 환영
'첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률 일부개정안(이하 첨생법)이 국회 본회의를 통과하면서 세포·유전자치료제(CGT) 등 바이오의약품 산업 성장에 속도가 붙을 전망이다. 2일 관련 업계에 따르면, 국회는 지난 1일 본회의를 열고 보건복지부 소관 법률인 첨생법에 대한 일부개정안을 통과시켰다. 개정안의 주요 골자는 '첨단재생의료 치료제도 도입' 및 '임상연구 대상자 범위 확대'다. 지난 2020년 8월 28일 시행된 첨생법은 세

제약·바이오
연세의료원, 美 AI 바이오벤처와 고형암 세포치료제 개발 나서
연세대학교 의료원(이하 연세의료원)이 고형암 세포치료제 개발에 박차를 가한다. 연세의료원은 전날 의료원장실에서 미국 바이오벤처기업 큐어 에이아이 테라퓨틱스(KURE AI Theraputics)와 세포치료제 개발 추진을 위한 협력 합의서를 체결했다고 31일 밝혔다. 체결식에는 윤동섭 의료원장, 이강영 기획조정실장, 최재영 의과학연구처장, 정재호 바이오클러스터추진단장와 큐어 에이아이 테라퓨틱스 황태현 연구개발 부문 총괄과 유진규 사업개발