한미약품은 차세대 면역조절 항암 혁신신약(LAPS IL-2 analog, 코드명: HM16390)의 임상 1상 진입을 위한 임상시험계획(IND)을 미국 식품의약국(FDA)에 신청했다고 3일 밝혔다.
HM16390은 면역세포의 분화와 증식을 통해 면역 기능을 조절하는 것으로 알려진 IL-2(인터루킨-2)를 차별화된 전략으로 새롭게 디자인한 IL-2 변이체로, 한미약품의 독자 플랫폼 기술인 '랩스커버리'를 적용해 효능과 안전성, 지속성을 극대화한 혁신 신약이다.
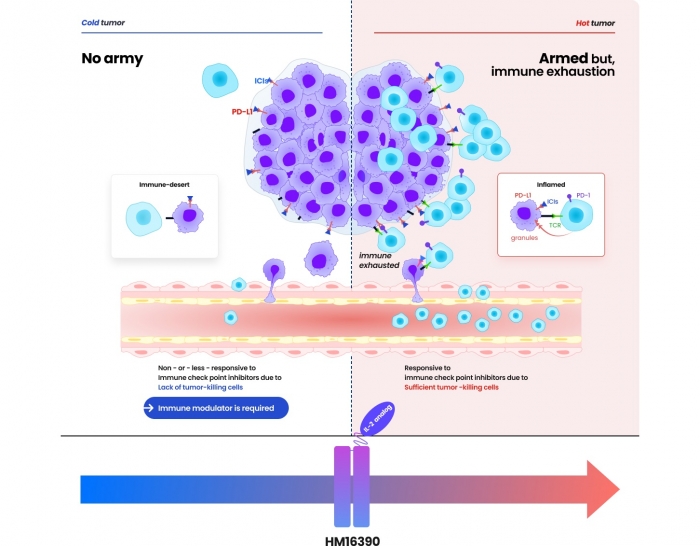
한미약품 측은 HM16390은 기존 IL-2 제제와는 차별화된 수용체 결합력을 통해 항암 효능이 크게 향상됐으며, 흑색종, 대장암뿐 아니라 신장암과 췌장암 동물 모델에서도 우수한 효능을 보여 다양한 진행성 또는 전이성 고형암에서 치료 효능을 기대할 수 있다고 설명했다. 특히 면역관문 억제제에 반응하지 않는 '차가운 종양(cold tumor)'에서도 치료 효과를 이끌어낼 수 있는 중요한 치료 옵션이 될 것으로 기대된다.
HM16390은 또 기존 IL-2 제제의 심각한 부작용이었던 혈관누출증후군 등을 대폭 개선하여 안전성을 높였다. 기존 IL-2 제제는 충분한 항암 효능을 위해 고용량 투여가 필요했으나, 이는 혈관누출증후군 등의 부작용을 유발했다. HM16390은 안전성을 확보하면서도 강력한 항암 효능을 발휘할 수 있도록 설계됐다.
한미약품은 HM16390이 단독 치료제로서도 효과가 뛰어날 것으로 기대하며, 면역관문 억제제와 병용 치료 시에는 치료 효과를 더욱 배가시킬 수 있을 것으로 보고 있다. 면역관문 억제제는 종양 주변의 면역억제 환경을 개선하여 면역세포가 암세포를 공격하도록 하는 데 효과적이지만, 일부 환자에서는 치료 효과가 나타나지 않거나 제한적으로 나타나는 경우가 있다. HM16390은 이러한 면역관문 억제제에 반응하지 않는 환자들에게도 새로운 치료 기회를 제공할 수 있을 것으로 기대된다.
한미약품 관계자는 "항종양 효능 극대화와 함께 안전성까지 개선된 HM16390은 단독요법은 물론 면역관문 억제제 병용시 종양미세환경을 변화시켜 치료 효과를 크게 높일 수 있을 것으로 기대된다"며 "기존 치료제에 반응하지 않는 암 환자에게 대안이 되는 차세대 면역조절 항암제 개발을 완수할 수 있도록 연구에 더욱 매진하겠다"고 말했다.

뉴스웨이 이병현 기자
bottlee@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지









댓글