1일 한국바이오협회 바이오경제연구센터에 따르면, FDA는 31일(현지시간) 신약(전문의약품), 제네릭, 바이오시밀러, 의료기기 제조 기업으로부터 받는 2025년 회계연도 허가심사수수료를 확정했다.
FDA는 매년 인플레이션, 심사 신청건수, 제조시설수, 심사자 고용 및 유지비 등을 감안해 이용자인 기업으로부터 받는 허가심사수수료를 책정하고 있으며, 이번 회계연도는 오는 10월1일부터 2025년 9월30일까지 적용된다.
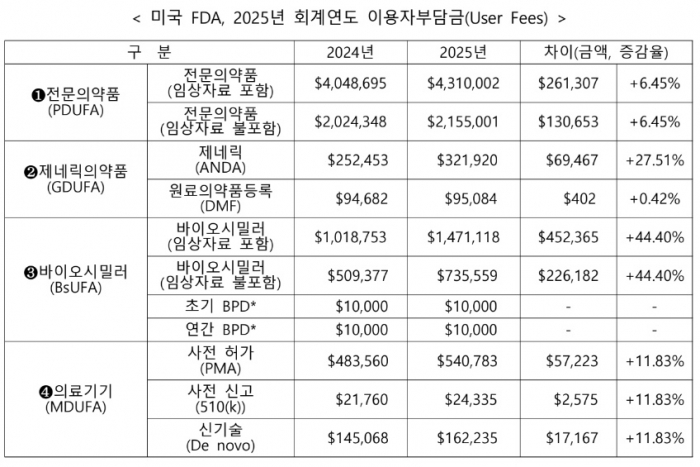
전문의약품에 대한 2025년도 허가심사 수수료는 전년도 대비 약 26만달러(3억5000만원)을 인상해 431만 달러(약 59억원)로 책정했다. 전문의약품에 대한 수수료는 지난해 사상 처음으로 400만 달러를 돌파했다.
제네릭의약품과 의료기기(사전허가·PMA 기준)는 각각 27.5%, 11.8% 인상돼 32만1920 달러(4억4058만원), 54만783 달러(7억4012만원)으로 책정됐다.
바이오시밀러 허가심사 수수료(임상자료 포함)는 147만1118 달러(20억1367만원)로 전년도 대비 44.4% 인상된다.
바이오시밀러 허가심사수수료가 가장 큰 폭으로 인상되는 이유는 지난 몇 년간 운영 준비금(operating reserve) 하향 조정으로 인한 추가 자금이 필요했기 때문이다.
FDA 측은 "지난 몇 년간 검토 업무량이 지속 증가했고 2025년에도 계속될 것으로 예상되기 때문에 이같이 인상했다"고 부연했다.
다만 바이오시밀러는 이용자부담금개정법(BsUFA)에 따라 수수료가 정해지고, 전문의약품과 마찬가지로 임상자료 심사 필요 여부에 따라 비용이 2배 이상 차이가 발생한다.
임상자료 불포함일 경우 수수료는 73만5559 달러(10억713만원)로 책정됐다. 인상률은 44.4%로 동일하다.
초기·연간 BPD(Biological product development)는 각각 1369만원이다. BPD는 바이오시밀러의 개발 및 승인을 신속하게 진행시키기 위한 FDA 심사관과 기업과의 공식적인 미팅 프로그램으로 초기(Initial BPD)와 연간(Annual BPD)으로 구분한다.
한편, 바이오시밀러는 바이오의약품 '수출 효자'로 꼽힌다. 지난해 바이오시밀러 수출액은 16억4276만 달러(약 2조2493억원)로, 바이오의약품 전체 수출액의 77.3%를 차지했다.
삼성바이오에피스는 세계 최대 의약품 시장인 미국에서 가장 많은 바이오시밀러인 8종을 허가 받았다.
셀트리온은 미국에서 레미케이드 바이오시밀러 '렘시마SC'를 신약으로 허가 받아 '짐펜트라'라는 제품명으로 판매 중이다.
휴미라 바이오시밀러 '유플라이마'도 지난해 FDA의 허가를 받은 이후 대형 처방약급여관리회사(PBM)와 처방집 등재 계약을 체결하는 등 시장 점유율 확대에 박차를 가하고 있다.
최근에는 '코센틱스' 바이오시밀러 'CT-P55'의 글로벌 임상 3상을 위한 임상시험계획서(IND)를 FDA에 제출하며 파이프라인 확대에 나서고 있다.

뉴스웨이 유수인 기자
suin@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지







댓글