리가켐·에이비엘바이오·동아에스티 등 개발자체 플랫폼·해외 법인·자회사 협업 전략 다양
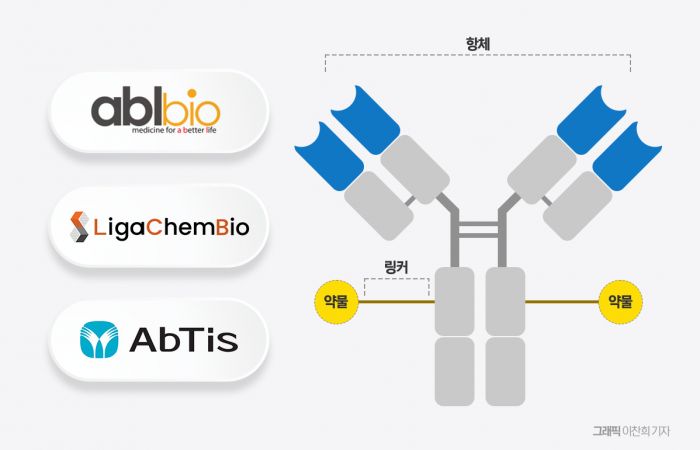
국내 제약·바이오 기업들이 항체약물접합체(ADC) 연구에 공을 들이고 있다. ADC란 암세포를 인식하는 항체(Antibody)와 세포독성 약물(Payload), 그리고 이들을 연결하는 링커로 구성된 기술이다. 리가켐바이오사이언스, 에이비엘바이오, 동아에스티(앱티스) 등이 주인공이다. 이들은 ADC 구성 요소 관련 자체 플랫폼부터 이중항체 ADC 등의 방안으로 ADC 개발에서 차별화를 뒀다.
OpenAI의 기술을 활용해 기사를 한 입 크기로 간결하게 요약합니다.
전체 기사를 읽지 않아도 요약만으로 핵심 내용을 쉽게 파악할 수 있습니다.
국내 제약·바이오 기업들이 항체약물접합체(ADC) 연구에 집중
리가켐바이오사이언스, 에이비엘바이오, 동아에스티(앱티스) 등이 주요 주자
각사 고유 플랫폼·기술로 차별화 시도
리가켐바이오, 9조원 규모 글로벌 기술이전 성과
현재 5개 파이프라인 임상 단계 진입
2027년까지 15개 추가 과제 임상 목표
에이비엘바이오, 네옥바이오 설립에 1400억원 투자
리가켐바이오, ConjuAll™ 플랫폼으로 치료지수 확장 및 맞춤형 페이로드 개발
익수다 테라퓨틱스에 기술이전한 HER2-ADC, 미국 FDA 임상 1상 승인
에이비엘바이오, 이중항체 ADC로 치료용량범위 개선 기대
동아에스티, 앱티스와 Claudin18.2 타깃 DA-3501 개발 및 임상 1상 진입
자체임상·기술이전 '병행'···선두기업 도약 제시
국내 ADC 관련 기업 중 가장 기술이전 실적이 많은 곳은 리가켐바이오사이언스이다. 리가켐바이오는 플랫폼과 파이프라인을 함께 기술이전하는 '패키지딜'에 더해 자체 임상을 병행해 ADC 글로벌 선두기업으로 도약할 것이라고 밝혔다.
리가켐바이오가 보유하고 있는 ADC 플랫폼 'ConjuAll™(콘쥬올)'이다. 콘쥬올은 항체 특정 부위에 원하는 수량의 페이로드를 부착할 수 있는 결합 방법부터 혈중안정성 및 암세포 특이적인 약물 방출 능력을 가진 링커, 신규 기전의 페이로드로 구성돼 있다.
콘쥬올을 활용하게 되면 넓은 치료지수(최대 허용 용량·MTD) 또는 중증 독성 발생하지 않는 최대 용량(HNSTD)/효능 확인 최소 용량(MED)를 확보할 수 있다는 게 리가켐바이오 측의 설명이다. 회사는 콘쥬올과 이를 기반으로 한 ADC 파이프라인을 글로벌 빅파마에 기술이전하며 계약 규모만 9조원이 넘는 성과를 거뒀다.
최근 들어 기술이전한 파이프라인의 개발 진행 상황도 뚜렷해지고 있다. 리가켐바이오가 영국 ADC 기업인 익수다 테라퓨틱스에 기술이전한 HER2-ADC 'IKS014'는 미국 식품의약국(FDA)으로부터 글로벌 임상 1상 임상시험계획승인(IND) 확대 승인을 받았다. IKS014는 유방암, 난소암, 담낭암, 식도암 등 고형암을 타깃으로 하는 HER2-ADC로, 리가켐의 콘쥬올과 MMAF 페이로드가 적용됐다.
익수다 측은 "초기 임상 결과 사전에 엔허투를 투약했지만 재발한 환자 군에서도 효능 결과를 확인했다"며 "2026년 하반기 중 임상 1상을 완료할 계획"이라고 밝혔다.
리가켐바이오는 기술이전에 더해 자체 임상도 함께할 계획이다. 김용주 리가켐바이오 대표는 "현재 5개의 파이프라인이 임상 단계에 진입했다"며 "2027년까지 15개의 추가 과제를 전임상 및 임상 단계에 진입하는 게 목표"라고 설명했다.
아울러 비캄포토테신(Non-Camptothecin), 표적단백질분해(TPD), 새 모달리티 기전 등의 페이로드도 개발할 계획이다.
페이로드는 ADC의 효과와 안전성에 중요한 요소로 작용하지만, 현재 사용 가능한 페이로드가 제한적이기 때문에 신규 페이로드 개발에 나서겠다는 것이다.
韓·美 투트랙 전략···'네옥바이오' 설립한 에이비엘
이중항체 플랫폼 기술로 잘 알려진 에이비엘바이오는 ADC 개발을 위해 미국 법인인 '네옥바이오'를 설립했다.
네옥바이오는 ▲ABL206 ▲ABL209를 비롯한 ADC의 연구를 주도한다는 게 특징이다. 앞선 두 파이프라인은 모두 이중항체 ADC로, ABL206은 오는 4분기, ABL209는 3분기 중에 임상 1상 임상시험계획승인(IND) 신청을 앞두고 있다.
두 파이프라인 모두 구체적인 타깃은 네옥바이오가 임상에 본격 진입한 후 1상 데이터가 확보됐을 때 공개될 예정이다.
회사 측은 이중항체 ADC의 상용화 사례가 아직 없다는 점에 주목했다. 항암제에서 효과를 보기 위해선 MED를 줄이고 치료용량범위(Therapeutic Window)를 증가시키는 게 중요한데, 이중항체 ADC는 기존 단일항체 ADC 대비 이 부분에서 개선 가능성이 크기 때문이다. 2026년 상반기 중 임상 1상 개시를 목표로 하고 있어, 빠른 임상 진입이 가능하다는 점을 강점으로 내세웠다.
네옥바이오의 초기 자금은 에이비엘바이오가 유상증자한 1400억원으로 마련됐다. 이후 필요한 자금은 네옥바이오가 미국 벤처캐피탈(VC)을 통해 자체 조달할 예정이며, 향후 글로벌 제약사에 매각도 고려 중인 것으로 알려졌다. 결국 에이비엘바이오는 기술이전 로열티와 미국 법인 엑싯 전략을 통해 '자체 개발 신약 기업'으로의 전환과 안정적인 성장을 추진하겠다는 것이다.
이외에도 에이비엘바이오는 비임상 단계의 ADC 후보물질을 다수 보유하고 있으며, 네옥바이오는 토퍼아이소머라제 I(topoisomerase I) 억제제 페이로드뿐만 아니라 신규 페이로드를 활용해 ADC 파이프라인을 꾸준히 확대해 나갈 예정이다.
앱티스 손잡은 동아에스티, 첫 ADC 임상 돌입
동아에스티는 자회사 앱티스와 함께 ADC 신약 후보물질을 개발 중이다. 양사가 개발 중인 DA-3501은 클라우딘18.2(Claudin18.2)를 타깃으로 하며, 위암 및 췌장암 등 고형암이 주요 적응증이다.
Claudin18.2의 경우 암 세포에서 발현되는 단백질로, 치료 옵션이 매우 제한적이라는 게 특징이다. 따라서 글로벌 빅파마들은 Claudin18.2를 타깃하는 ADC 개발에 집중하는 추세다.
DA-3501은 앱티스가 자체 개발한 플랫폼 '앱클릭'이 적용됐다. 앱클릭은 ADC 구성 요소 중 링커에 초점을 맞춘 플랫폼으로, 특정 위치에 약물을 선택적으로 결합할 수 있으며 항체-약물 비율(DAR)을 균일하게 할 수 있다는 게 핵심이다.
동아에스티는 지난달 DA-3501의 국내 임상 1상 진입을 위한 임상시험계획승인(IND)을 신청했다. 이는 동아에스티의 첫 ADC 파이프라인으로, 임상 진행 등 국내 및 글로벌 개발은 동아에스티가 주도적으로 추진할 계획이다.
관련기사

뉴스웨이 현정인 기자
jeongin0624@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지









댓글